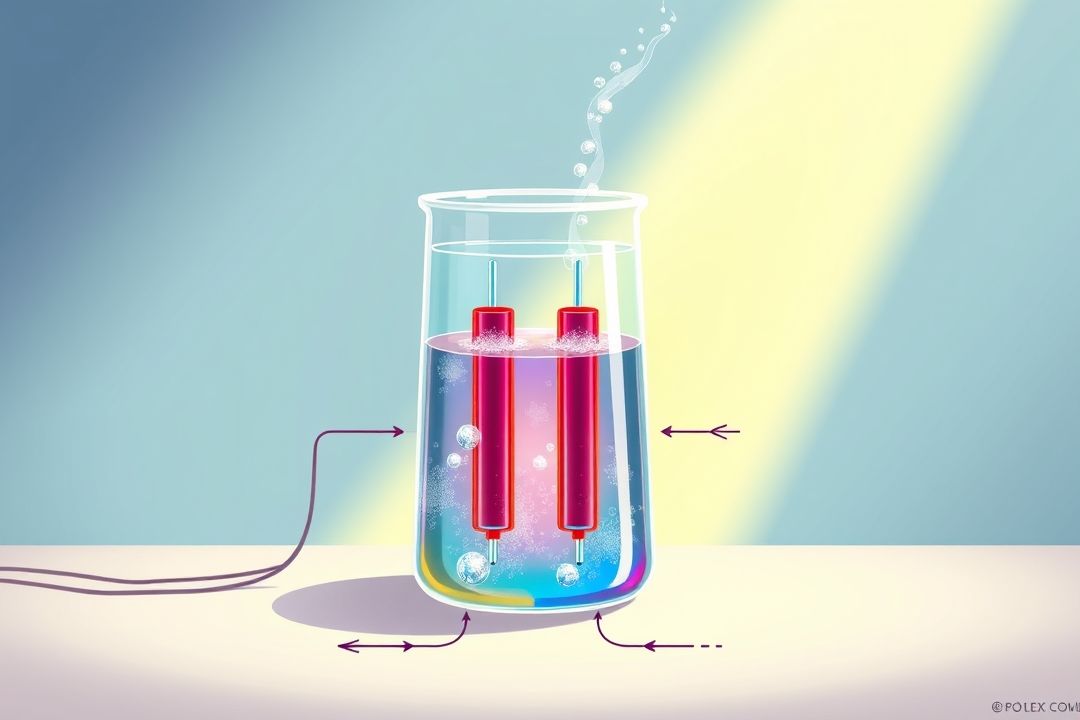
Электролитический процесс: что это такое и как он работает
Электролитический процесс — это важный химический процесс, который находит широкое применение в различных отраслях промышленности. Он используется для очистки металлов, извлечения веществ из растворов и даже для получения чистых газов. В этом посте мы подробно рассмотрим, что такое электролитический процесс, как он работает и где применяется.
Основные компоненты электролитического процесса
Для того чтобы электролитический процесс мог происходить, необходимы три ключевых компонента:
1. Электричество
Источник энергии, который запускает процесс.
2. Электролит
Вещество, содержащее свободные ионы, которые могут перемещаться под действием электрического тока.
3. Электроды
Два объекта, которые проводят электрический ток и участвуют в химических реакциях.
Когда электрический ток проходит через электролит, он вызывает химические реакции, которые в обычных условиях не происходили бы. Например, в процессе рафинирования металлов атомы нечистого вещества перемещаются к чистому катоду, где они осаждаются, образуя чистый металл.
Применение электролитического процесса в рафинировании металлов
Одним из наиболее распространенных применений электролитического процесса является рафинирование металлов. В этом процессе оба электрода обычно изготавливаются из того же металла, который необходимо очистить. Например, анод может быть сделан из нечистой руды или сплава, а катод — из чистого металла. Электролит содержит свободные ионы этого металла, которые находятся в растворе.
Когда на электроды подается электрический ток, ионы из раствора начинают перемещаться к соответствующим электродам. Положительно заряженные ионы (катионы) движутся к катоду, где они принимают электроны и осаждаются в виде чистого металла. В то же время отрицательно заряженные ионы (анионы) движутся к аноду, где они отдают электроны и могут участвовать в других химических реакциях.
Электролитический процесс также используется для покрытия одного металла другим. Этот метод называется гальванопокрытием и широко применяется в производстве для улучшения коррозионной стойкости и декоративных свойств изделий. В процессе гальванопокрытия на поверхность одного металла осаждается другой металл, что позволяет создать защитный слой.
Электролиз для получения чистых газов
Электролитический процесс также может быть использован для получения чистых газов, таких как водород и кислород. Вода, состоящая из водорода и кислорода, может быть разложена на эти компоненты с помощью электрического тока. Для этого анод и катод обычно изготавливаются из инертных материалов, таких как нержавеющая сталь.
Когда электрический ток проходит через воду, она распадается на кислород, который выделяется у анода, и водород, который выделяется у катода. Если установить сосуды для сбора газа на соответствующих электродах, можно получить чистый водород или кислород. Однако стоит отметить, что процесс электролиза


